
Олія чорного кмину з гомогенатом є унікальною формою олії насіння Nigella sativa L. (чорний кмин), отриманою шляхом поєднання технологій холодного віджиму та високозсувної гомогенізації з високим навантаженням на зріз. Такий підхід забезпечує не лише збереження, але й максимальне вивільнення та синергію біоактивних компонентів цільного насіння. Основна фармакологічна дія препарата зумовлена його головним компонентом — тимохіноном (TQ).
Препарат виявляє широкий спектр біологічної активності, підтвердженої численними доклінічними дослідженнями. Він виступає як:
– потужний антиоксидант;
– ефективний протизапальний засіб;
– антимікробний агент – проявляє активність проти бактерій (включаючи стійкі штами), грибів та паразитів;
– противірусний засіб;
– модулятор імунної системи;
– протидіабетичний засіб.
Ключові переваги лікарської форми:
– олія холодного віджиму виступає як носій ліпофільних сполук, забезпечуючи високу концентрацію тимохінону та інших термочутливих компонентів у їх природній формі;
– високозсувна гомогенізація пасти руйнує клітинні стінки насіння, вивільняючи гідрофільні біоактивні речовини (такі як алкалоїди, флавоноїди, сапоніни), які не переходять у звичайну олію. Це створює синергічний ефект і значно підвищує загальну біодоступність та широту фармакологічної дії агента.
Показання до застосування (на основі фармакологічних досліджень):
Завдяки багатогранному механізму дії, агент може розглядатися як допоміжний засіб у комплексній терапії та профілактиці широкого кола патологічних станів, пов’язаних із запаленням, оксидативним стресом, метаболічними порушеннями та інфекціями, зокрема захворювань серцево-судинної, дихальної, травної, нервової систем, а також цукрового діабету та деяких видів новоутворень.
Основні активні компоненти олії чорного кмину з гомогенатом
Ліпофільні (переважно з олії):
– тимохінон – головний біоактивний компонент, потужний антиоксидант, має протизапальні, протипухлинні, антимікробні та імуномодулюючі властивості; тимол – антисептик, протигрибкова та антигельмінтна дія;
– жирні кислоти: лінолева кислота (омега-6), олеїнова кислота (омега-9), пальмітинова кислота, альфа-ліноленова кислота (омега-3);
– жиророзчинні вітаміни та стероли: вітамін Е, фітостерин.
Гідроофільні та тверді (переважно з фракції пасти):
– алкалоїди (унікальні для чорного кмину): нігеліцин – анальгезуюча та седативна дія, нігелідин – протизапальна та спазмолітична, нігеламін;
– сапоніни – імуномодулююча та адаптогенна дія;
– флавоноїди – антиоксидантні та капіляростабілізуючі властивості, протизапальна дія;
– білки, пептиди та амінокислоти;
– поживні волокна (клітковина) – пребіотики, покращують перистальтику;
– мінерали (макро та мікроелементи): залізо, кальцій, калій, цинк, селен, магній, фосфор;
– водорозчинні вітаміни – комплекс вітамінів групи В;
– полісахариди – імуномодулюючі властивості.
Фармакологічні властивості олії чорного кмину з гомогенатом
Тимохінон, будучи одним з основних активних компонентів олії чорного кмину з гомогенатом, володіє вираженим протизапальним та антиоксидантним ефектом.
В якості протизапального компоненту тимохінон “працює” на молекулярному рівні, пригнічуючи основні запальні шляхи:
– блокує NF-κB – головний “перемикач” запалення. Тимохінон не дає йому активуватися, через що клітина не може виробляти прозапальні цитокіни (TNF-α, IL-1β, IL-6) та ферменти (COX-2 – циклоксигеназу-2), які викликають біль, набряк і пошкодження тканин;
– пригнічує COX-2 та LOX (ліпооксигеназу) – ферменти, які синтезують медіатори болю та запалення (простагландини, лейкотрієни);
– модулює інші шляхи: впливає на передачу сигналу через інфламосоми NLRP3 та шлях JAK-STAT, що призводить до загального зниження запальної відповіді. Антиоксидантна дія тимохінону здійснюється в декількох напрямках:
– пряме знешкодження вільних радикалів;
– підсилення власної антиоксидантної активності;
– збереження глутатіону.
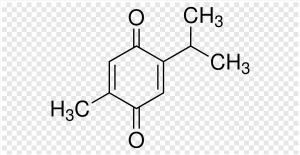 Тимохінон діє як потужний «ловитель» (scavenger) вільних радикалів завдяки своїй унікальній хімічній структурі та реакційній здатності.
Тимохінон діє як потужний «ловитель» (scavenger) вільних радикалів завдяки своїй унікальній хімічній структурі та реакційній здатності.
Тимохінон має бензохінонове ядро з двома карбонільними групами (C=O). Ця структура дозволяє йому:
– легко приймати електрони;
– вступати в реакції відновлення, перетворюючись на стабільніші форми (наприклад, тимогідрохінон).
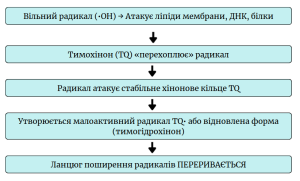
Механізм знешкодження тимохіноном вільних радикалів
-
Пряме переривання радикальних ланцюгів. Тимохінон безпосередньо реагує з високореактивними вільними радикалами (•OH, ROO•, O₂•⁻), передаючи їм електрон або атом водню. Утворений радикал тимохінону (TQ•) набагато менш реактивний і стабільніший, що припиняє ланцюгову реакцію пошкодження.
-
Хелатування іонів металів (непрямий механізм). Багато радикалів утворюються в реакціях Фентона за участю іонів переходних металів (Fe²⁺, Cu⁺). Тимохінон здатний хелатувати (зв’язувати) ці іони, роблячи їх неактивними і запобігаючи утворенню найнебезпечніших радикалів (наприклад, •OH з H₂O₂).
-
Регенерація інших антиоксидантів. Тимохінон може відновлювати інші антиоксиданти (наприклад, вітамін Е, вітамін С), які вже виконали свою роль, повертаючи їх у активну форму. Це продовжує загальний антиоксидантний захист.
Отже, тимохінон не просто “вбирає” вільні радикали, а хімічно їх трансформує в безпечні сполуки та блокує джерела їх утворення.
- Підсилення власної антиоксидантної активності тимохіноном відбувається на клітинно-ядерному рівні – він підвищує експресію генів власних антиоксидантних ферментів клітини:
– супероксиддисмутази (SOD) – перетворює супероксид (O₂•⁻) на менш шкідливу H₂O₂;
– каталази та глутатіонпероксидази (GPx) – розщеплюють H₂O₂ на воду. - Також тимохінон збільшує запас глутатіону (GSH) – головного клітинного антиоксиданта. Це здійснюється за шляхом:
– прямої стимуляції синтезу глутатіону через ключові ензими шляху біосинтезу глутатіону (активація Nrf2),
– підвищення активності та доступності компонентів для синтезу GSH – збільшення доступності цистеїну, захист та регенерація існуючого цистеїну,
– підвищення активності ферментів, що відновлюють GSH – глутатіонредуктази (GR), глутатіонпероксидази (GPx) та глутатіон-S-трансферази (GST).
Підсумовуючи – тимохінон діє як потужний регулятор і захисник на рівні клітинних сигнальних шляхів, одночасно пригнічуючи прозапальні механізми і активуючи захисні антиоксидантні системи. Таким чином він розриває замкнуте коло “окисний стрес → запалення → пошкодження тканин → новий окисний стрес”.
Механізм антиоксидантної дії
- Генетичний рівень: активація сигнального шляху Nrf2/ARE → транскрипція антиоксидантних генів. Це центральний механізм, описаний у більшості сучасних оглядів. Тимохінон викликає дисоціацію фактора транскрипції Nrf2 (nuclear factor erythroid 2–related factor 2) від його інгібітора Keap1 у цитоплазмі. Nrf2 переміщується в ядро та зв’язується з антиоксидантним відповідним елементом (ARE) у промоторних ділянках генів. Наслідок – підвищується транскрипція понад 200 генів, що кодують антиоксидантні ферменти:
– гемоксигеназа-1 (HO-1),
– глутатіон-S-трансфераза (GST),
– НАД(Ф)Н: хіноноксидоредуктаза (NQO1),
– SOD,
– CAT. -
Пряма антиоксидантна дія: скевенджер вільних радикалів. Тимохінон, завдяки своїй хіноновій структурі, здатний безпосередньо нейтралізувати вільні радикали:
– знешкодження супероксид-аніонів (O₂•⁻) та гідроксильних радикалів (•OH),
– інгібування перекисного окислення ліпідів у клітинних мембранах,
– зниження рівня малонового діальдегіду (MDA) — маркера оксидативного пошкодження. -
Активація АМРК та інших сигнальних шляхів. Тимохінон активує додаткові захисні механізми:
– шлях АМРК,
– SIRT1/AMPK,
– PGC-1α. -
Мітохондріально-спрямована антиоксидантна дія. Тимохінон є похідним 2-деметилпластохінону, що дозволяє йому легко відновлюватись дихальним ланцюгом мітохондрій. Накопичення тимохінону в мітохондріях призводить до стабілізації мембранного потенціалу, що захищає мітохондрії від оксиного пошкодження.
-
Відновлення і підтримка глутатіонової системи. Глутатіон (GSH) – головний внутрішньоклітинний антиоксидант:
– тимохінон відновлює знижений рівень глутатіону в умовах оксидативного стресу,
– зменшує рівень окисненого глутатіону, відновлюючи редокс-баланс,
– підвищує активність глутатіонпероксидази (GPx) та глутатіон-S-трансферази (GST). -
Зниження маркерів оксидативного стресу:
– MDA (малоновий даільдегід),
– LPO (перекисне окиснення ліпідів). -
Інгібування прозапальних шляхів, пов’язаних з оксидативним стресом:
– блокування NF-κB -тимохінон пригнічує ядерний фактор каппа-бі, знижуючи продукцію прозапальних цитокінів (TNF-α, IL-1β, IL-6),
– зниження COX-2 та iNOS – пригнічення ферментів, що продукують медіатори запалення,
– підвищення IL-10 – посилення продукції протизапального цитокіну.
Клінічне значення
Дослідження підтверджують, що тимохінон ефективно захищає від оксидативного стресу, спричиненого:
– важкими металами (кадмій, арсен, свинець),
– хіміотерапевтичними препаратами (доксорубіцин),
– ультрафіолетовим випромінюванням (UVA-індуковане пошкодження шкіри),
– нейротоксинами (модель хвороби Паркінсона, Альцгеймера).
Основні механізми протизапальної дії
- Блокування сигнального шляху NF-κB (ключовий механізм). Тимохінон блокує фосфорилювання та деградацію інгібіторного білка IκBα, в результаті чого NF-κB (субодиниця p65) залишається в цитоплазмі та не транслокується в ядро. Внаслідок цього пригнічується транскрипція понад 150 генів, що кодують прозапальні білки.
-
Пригнічення прозапальних ферментів та медіаторів:
– інгібування COX-2 – тимохінон знижує експресію COX-2 на рівні мРНК та білка, що призводить до зменшення синтезу простагландину E₂ (PGE₂);
– пригнічення iNOS – блокування індуцибельної NO-синтази зменшує продукцію оксиду азоту (NO);
– зниження прозапальних цитокінів (дослідження 2024 року підтвердило, що тимохінон значно знижує рівні TNF-α, HMGB1, IL-1β та IL-6 у макрофагах).
HMGB1 (High Mobility Group Box 1) — це унікальний білок, який виконує дві абсолютно різні функції залежно від свого розташування: у ядрі клітини він працює як структурний білок, а в позаклітинному просторі перетворюється на потужний прозапальний цитокін. -
Модуляція MAPK сигнальних шляхів. Тимохінон зменшує фосфорилювання p38 MAPK, JNK та Akt, але не впливає на ERK1/2, в результаті чого знижується передача запальних сигналів від клітинної мембрани до ядра.
-
Активація Nrf2/HO-1 антиоксидантного шляху. Тимохінон не тільки пригнічує запалення, але й активує захисні механізми через Nrf2, індукуючи експресію гемоксигенази-1 (HO-1), глутатіон-S-трансферази (GST) та NAD(P)H-хіноноксидоредуктази (NQO1). Це забезпечує цитопротекторний ефект та посилює загальну протизапальну дію.
-
Інгібування IRAK1 (кіназа-1, асоційована з рецептором інтерлейкіну-1) ! нова мішень ! Тимохінон безпосередньо пригнічує активність кінази IRAK1, яка є ключовим компонентом TLR-сигналінгу. Внаслідок цього пригнічується активація АР-1 та NF-κB шляхів, що призводить до значного зниження запальної відповіді.
IRAK1 (Interleukin-1 Receptor-Associated Kinase 1) — це ключова протеїнкіназа, яка діє як центральний передавач сигналу в системі вродженого імунітету. Його роль можна описати як молекулярний модератор запальної відповіді. IRAK1 — це не просто “перемикач” запалення, а специфічний регулятор, чия роль залежить від типу клітин: він незамінний для противірусного захисту, але може бути замінений іншими білками (IRAK2) при продукції “класичних” прозапальних цитокінів. IRAK1 відіграє вирішальну роль у противірусному захисті (через інтерферони) та патогенезі аутоімунних і запальних хвороб, що робить його важливою мішенню для фармакологічного втручання.
Клінічне значення. Оглядова стаття 2021 року підсумовує, що тимохінон ефективний при лікуванні: захворювань серця, респіраторних захворювань (астма, бронхіт), нейрозапальних процесів, цукрового діабету, артриту.
Основні механізми імуномодулюючої дії
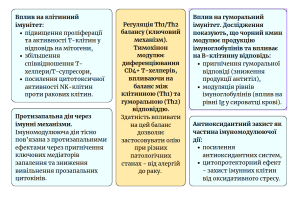
Механізм кардіопротекторної дії олії

Механізм протидіабетичної дії
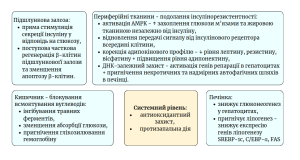
Протидіабетичний механізм. Першоджерело Arshad MT, Maqsood S, Ikram A, Abdullahi MA. Functional, Nutraceutical, and Pharmacological Properties of Black Seed. Food Sci Nutr. 2025 Aug 19;13(8):e70725. doi: 10.1002/fsn3.70725. PMID: 40842670; PMCID: PMC12365395
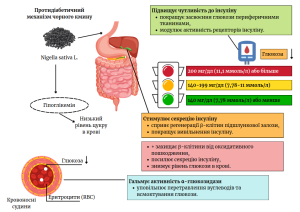
Механізм гепатопротекторної дії
- Нейтралізація оксидативного стресу. Тимохінон захищає печінку від пошкоджень через кілька антиоксидантних механізмів:
– інгібування перекисного окиснення ліпідів,
– підвищення рівня глутатіону,
– пряме зв’язування та нейтралізація вільних радикалів,
– активація антиоксидантних ферментів (SOD, CAT),
– відновлення та захист активності SOD та CAT при токсичному ураженні.
- Пригнічення запальних сигнальних шляхів. Тимохінон модулює ключові запальні шляхи, що захищає печінку:
– інгібування активності NF-kB,
– інгібування COX, LOX,
– пригнічення фосфорилювання (JNK, ERK, p38), індукованого токсинами,
– пригнічення експресії P2X7R та вивільнення IL-1α,
– інгібування фосфорилювання STAT3 при гострому ураження печінки. - Модуляція метаболічних шляхів та детоксикації. Тимохінон впливає на ключові ферменти метаболізму ксенобіотиків та енергетичний баланс:
– інгібування експресії CYP2E1 (ключовий фермент метаболізму токсинів),
– інгібування експресії CYP2E1 (ключовий фермент метаболізму токсинів),
– активація фосфорилювання АМРК,
– інгібування активації PI3K/mTOR сигналінгу,
– модуляція експресії PPARα та PPARγ (головні “вимикачі” метаболізму),
– зниження експресії CYP2B1 та CYP2B2 при токсичному ураженні. - Антиапоптична дія. Тимохінон запобігає загибелі клітин печінки через регуляцію апоптозу:
– підвищення експресії антиапоптичного білка Bcl-2,
– зниження експресії проапоптичного білка р53,
– зниження рівня активованої каспази-3,
– запобігання індукції проапоптичного білка Вах. - Пряме зв’язування токсичних метаболітів (зниження гіпербілірубінемії):
– інгібування експресії CYP2E1 (ключовий фермент метаболізму токсинів),
– пряме зв’язування білірубіну,
– інгібування зв’язування білірубіну з еритроцитами,
– значне зв’язування білірубіну в сироватці.
Клініко-лабораторні підтвердження. Дослідження на тваринних моделях підтверджують гепатопротекторний ефект через покращення функціональних показників печінки:
|
Показник |
Ефект тимохінону |
|
|
|
|
|
|
|
|
|
|
|
|
Механізм противірусної дії – вплив на ключові етапи життєвого циклу вірусу
- Пряма противірусна дія – пригнічення здатності вірусу до реплікації:
– інгібування вірусних протеаз за рахунок можливості тимохінону зв’язуватись з активним центром ферменту, блокуючи його роботу, що робить неможливим розмноження вірусу в клітині,
– вплив на клітинні сигнальні шляхи, необхідні вірусу для власної реплікації (Rho GTPase, PI3K-AKT та MAPK/ERK),
– пригнічення інших вірусних ферментів (інтеграза, протеаза та РНК-полімераза), що є критично важливими для життєвого циклу різних вірусів (гепатит С, ВІЛ). - Блокування проникнення вірусу в клітину:
– сполуки чорного кмину (тимохінон, дитимохінон, нігеллідин та α-гедерин з пасти) здатні зв’язуватися з рецептором ангіотензинперетворювального ферменту 2 (ACE2) на поверхні клітин,
– блокування spike-білка – тимохінон також може зв’язуватися з S-білком (spike protein) вірусу, заважаючи вірусу “зачепитися” за клітину,
– інгібування клітинного ферменту ТМРRSS2, необхідного для активації деяких вірусів. - >Імуномодулююча дія (контроль запалення):
– підвищення активності імунних клітин – лімфоцитів, NK-кілерів та макрофагів,
– зменшує вироблення прозапальних цитокінів (інтерлейкінів IL-6, IL-1β, IL-2, IL-4, IL-12 та фактору некрозу пухлин TNF-α), які є головними винуватцями “цитокінового шторму”,
– модуляція оксиду азоту та АФК.
Сполуки, отримані з N. sativa, можуть блокувати кілька етапів життєвого циклу SARS-CoV-2, включаючи проникнення, реплікацію та транскрипцію, що робить рослину багатим джерелом біоактивних сполук проти SARS-CoV-2. Лікування N. sativa може мати численні переваги для пацієнтів, інфікованих HCV (вірусу гепатиту С), шляхом зменшення реплікації вірусу та одночасного полегшення таких факторів, як оксидативний стрес та діабет, що сприяють прогресуванню вірусу. Результати демонструють потужну противірусну активність олії чорного кмину проти CMV (цитомегаловірус), яка, найімовірніше, опосередкована його імуностимулюючим ефектом (збільшення рівня IFN-γ у сироватці крові, макрофагів та CD4+ T-клітин), хоча не можна виключати прямий наслідок впливу екстракту на сам вірус.
Перше експериментальне підтвердження цієї багаторівневої дії було отримано в дослідженні in vitro 2024 року, яке показало, що тимохінон ефективно пригнічує розмноження вірусу SARS-CoV-2 (омікрон) як при профілактичному застосуванні, так і при лікуванні вже інфікованих клітин. Це свідчить про його високий потенціал як універсального противірусного агента.
Alagie Jassey, Zuha Imtiyaz, Sheriffo Jassey, Mufeed Imtiyaz, Saiema Rasool. Antiviral effects of black seeds: Effect on COVID-19. Elsevier, 2022, Pages 387-404. ISBN 9780128244623 https://doi.org/10.1016/B978-0-12-824462-3.00004-4
Механізм антиканцерогенної дії
- Індукція апоптозу – внутрішній (мітохондріальний) та зовнішній (рецептор-опосередкований) шляхи:
– активація мітохондріального шляху – тимохінон порушує цілісність мітохондріальної мембрани, що призводить до вивільнення цитохрому с та активації каспаз,
– регуляція балансу білків родини Bcl-2 – знижує рівень антиапоптичних та підвищує рівень проапоптичних білків,
– активація зовнішнього шляху – підвищує експресію рецепторів смерті, активує каспазу-8. - Зупинка клітинного циклу (тимохінон здатен зупиняти безконтрольний поділ ракових клітин):
– блокування фаз клітинного циклу (G1/S або G2/M),
– пригнічення сигнальних шляхів, що контролюють ріст клітин (EGFR/ERK1/2 та PI3K/Akt). - Інгібування NF-kB та запального мікрооточення пухлин:
– блокує активацію NF-kB,
– знижує експресію генів-мішеней NF-kB. - Зменшення інвазії та метастазування – пригнічення активності матриксних металопротеїназ (ММР-2, ММР-9) – ферментів, що руйнують позаклітинний матрикс, дозволяючи раковим клітинам проникати в навколишні тканини та кровотік.
- >Індукція оксидативного стресу (вибіркова токсичність) – тимохінон діє як прооксидант у ракових клітинах, що призводить до надмірного накопичення АФК у ракових клітинах, викликаючи апоптоз.
- Інгібування ангіогенезу:
– знижує експресію VEGF (фактор росту ендотелію судин),
– пригнічує проліферацію та міграцію ендотеліальних судин,
– блокує сигнальний шлях PI3K/Akt/mTOR, критичний для виживання ендотелію. - Синергія з хіміотерапією та подолання резистентності:
– посилення дії хіміопрепаратів (топотекан, цисплатин та доцетаксел),
– подолання резистентності – впливаючи на різні сигнальні шляхи, тимохінон може робити ракові клітини, стійкі до хіміотерапії, чутливими до лікування. - Епігенетична регуляція (інгібування гістонових деацетилаз) — досліджується.
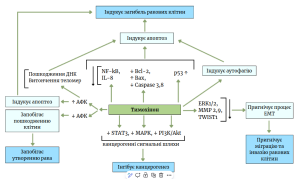
Asaduzzaman Khan M, Tania M, Fu S, Fu J. Thymoquinone, as an anticancer molecule: from basic research to clinical investigation. Oncotarget. 2017 Apr 18;8(31):51907-51919. doi: 10.18632/oncotarget.17206. PMID: 28881699; PMCID: PMC5584300
Епітеліально-мезенхімальний перехід (ЕМП) — це біологічний процес, при якому клітини епітелію втрачають свої характерні ознаки (полярність, здатність до щільного з’єднання) і набувають мезенхімальних властивостей (рухливість, інвазивність). Тобто, ЕМП перетворює “осілі” ракові клітини на “мандрівників”, здатних поширюватися по організму та утворювати метастази.
Антиканцерогенна активність чорного кмину – механізм дії 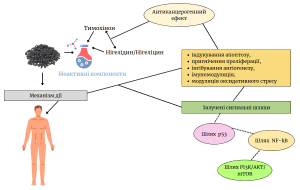
Arshad MT, Maqsood S, Ikram A, Abdullahi MA. Functional, Nutraceutical, and Pharmacological Properties of Black Seed. Food Sci Nutr. 2025 Aug 19;13(8):e70725. doi: 10.1002/fsn3.70725. PMID: 40842670; PMCID: PMC12365395
Механізм антибактеріальної дії – пошкодження ключових структур бактеріальної клітини 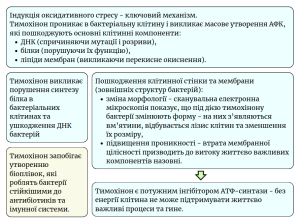
Ефективність тимохінону підтверджена проти широкого спектру бактерій, включаючи стійкі штами, такі як метицилін-резистентний золотистий стафілокок та лікарсько-стійкі мікобактерії, Staphylococcus aureus та Yersinia enterocolitica.
Механізм антигістамінної дії
- Стабілізація мембран опасистих клітин (мастоцитів) – пригнічення вивільнення гістаміну. Мастоцити є головним “депо” гістаміну в організмі. Під дією алергену вони викидають вміст гранул, що призводить до масивного вивільнення гістаміну та розвитку алергічної реакції. Профілактичний ефект – відсоток інгібування значно вищий, коли препарат контактував з клітинами до введення антигену.
- Блокування гістамінових рецепторів на клітинах-мішенях – антагонізм до гістаміну. Навіть якщо частина гістаміну вивільнилася, тимохінон здатен блокувати його дію на клітини-мішені (гладенькі м’язи бронхів, судин, кишечника).
- Модуляція імунної відповіді (Th1/Th2 баланс). Алергічні реакції тіснопов’язані з дисбалансом Т-хелперних клітин – надмірною активністю Th2-клітин (які продукують інтерлейкіни IL-4, IL-5, IL-13, що стимулюють вироблення IgE) та пригніченням Th1-клітин.
– Дослідження на мишах з алергічним ринітом показало, що водний екстракт чорного кмину стимулював продукцію Th1-цитокінів та регуляторних Treg і пригнічував вивільнення Th2-цитокінів та гістаміну в слизовій носової порожнини та сироватці крові.
– Тимохінон знижує рівень прозапальних цитокінів TNF-α та IL-1β, які посилюють алергічне запалення.
Паста, отримана шляхом високозсувної гомогенізації робить біодоступними алкалоїди (нігеліцин, нігеллідин), поліфеноли та алкалоїди, які мають власну антигістамінну активність та модулюють імунну відповідь, відновлюючи баланс Th1/Th2 та зменшуючи продукцію IgE. Отже, олія чорного кмину може бути ефективним засобом для лікування алергічних захворювань, таких як бронхіальна астма та алергічний риніт.
Механізм протипаразитарної дії – багаторівнева атака
- Рівень 1. Метаболічний (призводить до порушення енергозабезпечення паразита):
– окисний стрес – тимохінон діє як прооксидант щодо клітин паразитів, але як антиоксидант щодо клітин хазяїна – зниження рівня відновленого глутатіону, порушення балансу GSH/GSSG, інгібування активності глутатіонпероксидази (GPx), інгібування активності SOD,
– інгібування ключових ферментів паразита (гамма-глутамілтранспептидаза, GGT) призводить до порушення надходження амінокислот та метаболічного голодування. - Рівень 2. Структурний (призводить до втрати цілісності паразита). Тегумент – зовнішній покрив багатьох паразитів, який виконує захисну, поживну та видільну функції. Електронна мікроскопія показала виражені порушення тегументу, втрату поверхневих кільцеподібних структур та ерозію в ділянці задніх сосочків.
- Рівень 3. Генетичний (призводить до загибелі клітин). Тимохінон здатен запускати апоптичні процеси в клітинах паразитів:
– фрагментація ДНК,
– зупинка клітинного циклу,
– NO-залежний апоптоз.
- Рівень 4. Функціональний. Тимохінон викликає значне дозозалежне зниження рухливості паразитів, що є критичним для здатності утримуватись в організмі хазяїна.
Дослідження підтверджують ефективність тимохінону та екстрактів чорного кмину проти різних груп паразитів: лейшманій – з індукцією апоптозу та зупинкою клітинного циклу, трематод – через пригнічення антиоксидантних ферментів, шистосом – зі зниженням кількості паразитів та гранульом, нематод – з викликанням незворотного паралічу. Гідрофільні сполуки пасти (алкалоїди, сапоніни, флавоноїди) мають власну антипаразитарну активність і підсилюють дію тимохінону.
Механізм протигрибкової дії
- Рівень 1. Метаболічний (призводить до порушення енергозабезпечення):
– окисний стрес – тимохінон діє як прооксидант, генеруючи масове утворення вільних радикалів у клітинах грибів, знижує рівень глутатіону (GSH),
– інгібування ключових метаболічних ферментів (ізоцитратліази, ICL). - Рівень 2. Структурний (призводить до втрати цілісності). Описано основні морфологічні зміни патогенних грибів під дією олії чорного кмину:
– пошкодження клітинної стінки та плазматичної мембрани – порушення бар’єрної функції,
– зміни в мембранних органелах (особливо ядрі та мітохондріях) – призводить до порушення поділу та енергозабезпечення,
– лізис клітин – повне руйнування грибних клітин.
- Рівень 3. Вірулентний (втрата здатності до інвазії):
– пригнічення утворення біоплівок та гіф (тимохінон блокує перехід дріжджової форми у нитчасту – ключовий фактор інвазивності Candida albicans),
– зниження експресії генів адгезії – тимохінон пригнічує гени ALS1 та HWP1, які відповідають за прикріплення грибів до поверхонь.
Дослідження підтверджують ефективність тимохінону та екстрактів чорного кмину проти різних груп грибів: дерматофіти (Trichophyton mentagrophytes, Microsporum canis, Microsporum gypseum), дріжджі (Candida albicans, Candida glabrata), плісняві гриби (Aspergillus spp.).
При внутрішньому застосуванні олія може застосовуватись в якості допоміжного засобу при широкому спектрі захворювань завдяки своїм протизапальним, антиоксидантним, імуномодулюючим та метаболічним ефектам.
- Серцево-судинна система:
– артеріальна гіпертензія (для зниження тиску),
– атеросклероз, ішемічна хвороба серця,
– профілактика тромбозів. - Ендокринна система та обмін речовин:
– цукровий діабет 2 типу (для покращення контролю глікемії, зниження рівня цукру натще та глікованого гемоглобіну),
– метаболічний синдром, надмірна вага (для покращення ліпідного профілю, зниження холестерину, ЛПНЩ, тригліцеридів),
– дисліпідемія. - Вірусні інфекції:
– респіраторні інфекції: коронавіруси (229E, OC43, SARS-CoV-2), вірус парагрипу птахів (NDV), грип, респіраторно-синцитіальний вірус (RSV),
– віруси гепатиту С, В,
– ВІЛ. - Травна система:
– гастрит (для зменшення печії, нудоти, загоєння слизової),
– виразкова хвороба шлунка (допоміжний засіб для загоєння),
– панкреатит у стадії ремісії (для зменшення дискомфорту та метеоризму),
– порушення травлення, глистяні інвазії. - Дихальна система:
– бронхіт, пневмонія, ГРВІ, кашель (в якості відхаркувального, бактерицидного та протизапального засобу). - Запальні та аутоімунні захворювання:
– алергічні захворювання – алергічний риніт, атопічний дерматит, астма,
– ревматоїдний артрит (для зменшення болю, набряку та маркерів запалення). - Онкологічні захворювання (як ад’ювантна терапія) – в якості засобу, що потенційно може підвищувати ефективність хіміотерапії та зменшувати її токсичні побічні ефекти завдяки потужній антиоксидантній дії. Потребує подальших клінічних досліджень.
- Неврологічні захворювання: діабетична периферична нейропатія (для зменшення больового синдрому та покращення функції нервів – активні клінічні дослідження).
- Гінекологія: синдром полікістозних яєчників (СПКЯ) (для покращення гормонального балансу, зменшення об’єму яєчників та регуляції менструального циклу).
Список літератури:
-
Asha Caroline Cyril, Najma Mohamed Ali, Anagha Nelliyulla Parambath, Cijo George Vazhappilly, Reem Kais Jan, Noushad Karuvantevida, Haneen Aburamadan, Yosra Lozon, Rajan Radhakrishnan. – Nigella sativa and its chemical constituents: pre-clinical and clinical evidence for their potential anti-SARS-CoV-2 effects. Inflammopharmacologyю – Ausgabe 1/2024.
-
Chaieb K, Kouidhi B, Jrah H, Mahdouani K, Bakhrouf A. Antibacterial activity of Thymoquinone, an active principle of Nigella sativa and its potency to prevent bacterial biofilm formation. BMC Complement Altern Med. 2011 Apr 13;11:29. doi: 10.1186/1472-6882-11-29. PMID: 21489272; PMCID: PMC3095572.
-
Forouzanfar F., Bazzaz BS., Hosseinzadeh H. Black cumin (Nigella sativa) and its constituent (thymoquinone): a review on antimicrobial effects. Iran J Basic Med Sci. 2014 Dec;17(12):929-38. PMID: 25859296; PMCID: PMC4387228.
-
Hina Usmani, Saloni Malik, Anshu Arya, Pintu K. Mahto, Ravi Kant, Ruchi Dua, Girish Sindhwani, Anissa Atif Mirza and Prasanna Kumar Panda. Effects of Active Compounds of Nigella sativa in COVID-19: A Narrative Review. Recent Advances in Anti-Infective Drug Discovery, Volume 19, Issue 1, Apr 2024, p. 3 – 11. DOI:https://doi.org/10.2174/2772434418666230222140805.
-
Abo-Neima, S.E., El-Sheekh, M.M., Al-Zaban, M.I. et al. Antibacterial and anti-corona virus (229E) activity of Nigella sativa oil combined with photodynamic therapy based on methylene blue in wound infection: in vitro and in vivo study. BMC Microbiol 23, 274 (2023). https://doi.org/10.1186/s12866-023-03018-1.
-
Amaj A. Laskar, Masood A. Khan, Arshad H. Rahmani, Sana Fatima, Hina Younus. Thymoquinone, an active constituent of Nigella sativa seeds, binds with bilirubin and protects mice from hyperbilirubinemia and cyclophosphamide-induced hepatotoxicity. Biochimie, 2016, Volume 127, Pages 205-213. ISSN 0300-9084. https://doi.org/10.1016/j.biochi.2016.05.020.
-
Naina M. P. Maideen, Rajkapoor Balasubramanian and Arun Shanmugam. A Narrative Review on the Potential of Black Seeds (Nigella Sativa) in the Management of West Nile Virus Infection. Current Nutrition & Food Science, Volume 20, Issue 8, Oct 2024, p. 908 – 913. ISSN: 1573-4013. https://doi.org/10.2174/0115734013251160230921114603.
-
Naina Mohamed Pakkir Maideen, Rajkapoor Balasubramanian, Kumar Balasubramanian, Mohamed Harsath Jahir Hussain, Mohamed Fahath Shahul Hameed, Rethesh Senthil. Clinical and In vitro Data Shed New Light on the Therapeutic Advantages of Black Seeds (Nigella sativa) for the Treatment of Hepatitis C and Hepatitis B Viral Infections. Infectious Disorders – Drug Targets, Volume 25, Issue 6, 2025. ISSN 1871-5265. https://doi.org/10.2174/0118715265331112250115061024.
-
Al-Mubarak, Firas Taha Mansour; Hizam, Manar Mohammed1; Faleh Hashem Al-Gorani, Amal; Abood Al-Masoudi, Wasfi. Antiviral Effectiveness of Nigella sativa Oil on LaSota Strain of Newcastle Disease Virus In Vitro. Medical Journal of Babylon 21(Suppl 1):p S101-S106, June 2024. | DOI: 10.4103/mjbl.mjbl_249_23
-
Mollazadeh H, Hosseinzadeh H. The protective effect of Nigella sativa against liver injury: a review. Iran J Basic Med Sci. 2014 Dec;17(12):958-66. PMID: 25859299; PMCID: PMC4387231.
-
Goel S, Mishra P. Thymoquinone inhibits biofilm formation and has selective antibacterial activity due to ROS generation. Appl Microbiol Biotechnol. 2018 Feb;102(4):1955-1967. doi: 10.1007/s00253-018-8736-8. Epub 2018 Jan 22. PMID: 29356869.
-
Heena Tabassum, Asad Ahmad, Iffat Z. Ahmad. Nigella sativa L. and Its Bioactive Constituents as Hepatoprotectant: A Review. Current Pharmaceutical Biotechnology; Volume 19, Issue 1, 2018. DOI: 10.2174/1389201019666180427110007.
-
Majdalawieh AF, Fayyad MW. Immunomodulatory and anti-inflammatory action of Nigella sativa and thymoquinone: A comprehensive review. Int Immunopharmacol. 2015 Sep;28(1):295-304. doi: 10.1016/j.intimp.2015.06.023. Epub 2015 Jun 26. PMID: 26117430.
-
Ojueromi OO, Oboh G, Ademosun AO. Black Seed (Nigella sativa): A Favourable Alternative Therapy for Inflammatory and Immune System Disorders. Inflammopharmacology. 2022 Oct;30(5):1623-1643. doi: 10.1007/s10787-022-01035-6. Epub 2022 Aug 16. PMID: 35972596.







Залишити коментар