Исследование цитотоксического и антивирусного действия препарата Арекур на модельных системах іn vitro
Исследование проведено согласно ГФУ для определения активности интерферона. В модельной тест-системе №1 использовали клетки линии L929 (фибробласты мышей) и РНК-содержащий вирус везикулярного стоматита (ВВС, АТСС №VR-158) с инфекционным титром не менее 105 ТЦД50/0,1 мл. В модельной тест-системе №2 использовали клетки линии МА-104 (эпителиоподобная культура клеток, полученная из почек эмбриона зелёной макаки) и ДНК-содержащий вирус простого герпеса 1/2 типа (ВПГ -1/2, АТСС № VR-1493) с инфекционным титром не менее 104 ТЦД50/0,1 мл. Приведенные тест-системы соответствуют требованиям USP «Draft Guidance for Industry on Analytical Procedures and Methods Validation for Drugs and Biologics; Availability, 2014».
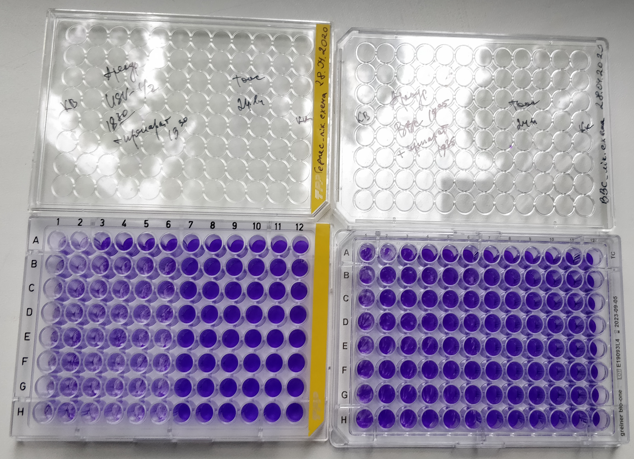
Оценка антивирусного действия различных концентраций субстанции препарата Арекур, приготовленных ex tempore на физиологическом растворе (ФР) проведена путем определения количества живых клеток в лунке, после их окрашивания кристаллическим фиолетовым [Saotome K, Morita H, Umeda M. Cytotoxicity test with simplified crystal violet staining method using microtitre plates and its application to injection drugs // Toxicol In Vitro. – 1989. – Vol.3, № 4. – P. 317–321. PMID: 20702298]. Через 24 ч после инфицирования проводили учет цитопатического действия вируса: после удаления из лунок надосадочной жидкости в дезраствор и к клеткам вносили 0,2% раствор красителя Crystal Violet («Sigma», США) в 2 % этаноле. Через 15 мин краситель удаляли, а окрашенный монослой клеток промывали под проточной водой. Оптическую плотность окрашенных клеток измеряли при длине волны 540 нм. Полученные результаты принимали во внимание только в том случае, когда в контрольных культурах, не содержащих вируса, цитодеструктивные изменения отсутствовали, а в контроле вируса наблюдали полную деструкцию клеток. Изучение антивирусного действия веществ проводили при 24-часовом контакте клеток с веществами, которые вносили через 40 мин после инфицирования тест-вирусом. Схема внесения образцов и проведения эксперимента, приведены ниже.
| З | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| A | КВ | Вирус +
Плацебо |
Вирус + А 1230 | Вирус + А 1230 | Вирус + А 1230 | Вирус + А 1230 | Плацебо | А 1230
|
А 1230
|
А 1230
|
А 1230
|
КК |
| B | КВ | Вирус +
Плацебо |
Вирус + А 123 | Вирус + А 123 | Вирус + А 123 | Вирус + А 123 | Плацебо | А 123 | А 123 | А 123 | А 123 | КК |
| C | КВ | Вирус +
Плацебо |
Вирус + А 12,3 | Вирус + А 12,3 | Вирус + А 12,3 | Вирус + А 12,3 | Плацебо | А 12,3 | А 12,3 | А 12,3 | А 12,3 | КК |
| D | КВ | Вирус +
Плацебо |
Вирус + А 1,23 | Вирус + А 1,23 | Вирус + А 1,23 | Вирус + А 1,23 | Плацебо | А 1,23 | А 1,23 | А 1,23 | А 1,23 | КК |
| E | КВ | Вирус +
Плацебо |
Вирус + А 0,123 | Вирус + А 0,123 | Вирус + А 0,123 | Вирус + А 0,123 | Плацебо | А 0,123 | А 0,123 | А 0,123 | А 0,123 | КК |
| F | КВ | Вирус +
Плацебо |
Вирус + А 0,012 | Вирус + А 0,012 | Вирус + А 0,012 | Вирус + А 0,012 | Плацебо | А 0,012 | А 0,012 | А 0,012 | А 0,012 | КК |
| G | КВ | Вирус +
Плацебо |
Вирус + А 0,001 | Вирус + А 0,001 | Вирус + А 0,001 | Вирус + А 0,001 | Плацебо | А 0,001 | А 0,001 | А 0,001 | А 0,001 | КК |
| H | КВ | Вирус +
Плацебо |
Вирус + А 0,0001 | Вирус + А 0,0001 | Вирус + А 0,0001 | Вирус + А 0,0001 | Плацебо | А 0,0001 | А 0,0001 | А 0,0001 | А 0,0001 | КК |
Условные обозначения: КВ – контроль вируса; КК – контроль клеток; Плацебо – растворитель (0,9% раствор натрия хлорида, изотоничен) А 1230 – субстанция препарат Арекур в концентрации 1230 мкг/мл культуральной среды).
В исследовании определено антивирусное действие субстанции препарата Арекур против 2-х разных вирусов: РНК-содержащего вируса везикулярного стоматита (ВВС) и ДНК-содержащего вируса простого герпеса ½ типа (ВПГ-1/2). В диапазоне эффективных концентраций субстанции препарата Арекур установлено СС50 – концентрацию субстанции препарата, вызывающую разрушения монослоя клеток на 50%, ЕC50 – эффективную концентрацию субстанции препарата (мкг/мл), необходимую для подавления цитопатического эффекта вируса на 50% и химио- терапевтический индекс (ХТИ) – отношение СС50 к ЕС50. Результаты исследования представлены в виде диаграмм, таблиц и фото изображений проведенного исследования при тестировании токсичности и окраски кристаллическим фиолетовым в рамках эксперимента по определению антивирусной активности субстанции препарата Арекур вместе с первичными данными. Проведено статистическую обработку полученных данных с применением методов непараметрической статистики, в частности определены медиана, первый и трeтий интeрквартильний размах.
Результаты изучения токсичности и антивирусной активности субстанции препарата Арекур в модельной системе L929 / ВВС
Полученные результаты антивирусной активности субстанции препарата Арекур представлены на графике (см. рис. 1).
Следует обратить внимание, что параллельно, в одной и той же системе, была изучена токсичность исследуемых образцов: схема применения препарата предусматривала его 24 ч контакт с монослоем клеток. Критерием токсичности вещества является значение СС50. Для образца субстанции препарата Арекур СС50 определить не удалось, поскольку концентрация 500 мкг/мл не вызывала каких-либо изменений в монослое клеток за 24 час. Показано наличие антивирусной активности у образцов с различной концентрацией субстанции препарата Арекур, приготовленных на физиологическом растворе.
Рисунок 1. Применение субстанции препарата Арекур в модельной системе L929/ВВС. Условные обозначения: контроль клеток – количество интактных клеток линии L929; токсичность ФР – количество клеток линии L929 после контакта с ФР на протяжении 24 ч; токсичность субстанции препарата Арекур – количество клеток линии L929 после контакта с субстанцией препарата Арекур на протяжении 24 ч; контроль ВВС – количество клеток линии L929 через 24 ч после инфицирования вирусом ВВС; антивирусная активность ФР – количество клеток линии L929 после инфицирования вирусом ВВС и обработки клеток ФР на протяжении 24 ч; антиВВС активность субстанции препарата Арекур – количество клеток линии L929 после инфицирования вирусом ВВС и обработки клеток субстанцией препарата Арекур на протяжении 24 ч; % живых клеток – количество адгезированных живых клеток линии L929 относительно интактных, принятых за 100%.
ЕС50 – в модельной системе L929/ВВС составила 10 мкг/мл субстанции препарата Арекур. Для расчета химиотерапевтического индекса (ХТИ), как отношения СС50 к ЕС50, необходимо использовать значение СС50, которое в данном блоке исследований установить не удалось, поскольку максимально изученная концентрация субстанции препарата Арекур 500 мкг/мл не оказывала какого-либо токсического действия на клетки. То есть, учитывая, что СС50 однозначно больше, чем 500 мкг/мл, есть все основания предполагать, что ХТИ субстанции препарата Арекур вероятно больше, чем 500/10 = 50. Полученные данные свидетельствуют о значительном антивирусном потенциале препарата Арекур в условиях его лечебного применения против РНК-содержащих вирусов, в том числе семейства Rhabdoviridae.
Таким образом, субстанция препарата Арекур в модельной системе L929/ВВС проявляет антивирусную активность, ХТИ препарата выше 50. Указанная величина (значительно выше показателя ХТИ, допускающего рассмотрение соединений, как перспективных антивирусных) свидетельствует о наличии антивирусной активности у препарата Арекур.
Результаты изучения токсичности и антивирусной активности субстанции препарата Арекур в модельной системе МА-104 / ВПГ-1/2
Полученные результаты влияния различных концентраций субстанции препарата Арекур, приготовленных на физиологическом растворе, на жизнеспособность и антивирусную резистентность клеток МА-104, инфицированных ВПГ-1/2, графически представлены на Рис. 2.
Прежде всего, следует отметить, что субстанция препарата Арекур в максимальной исследованной концентрации – 500 мкг/мл не проявляла токсического действия в культуре клеток МА-104 при 24 час. контакта с клетками.
Рисунок 2. Применение субстанции препарата Арекур в модельной системе МА-104/ВПГ-1/2. Условные обозначения: контроль клеток – количество интактных клеток линии МА-104; токсичность ФР – количество клеток линии МА-104 после контакта с ФР на протяжении 24 ч; токсичность субстанции препарата Арекур – количество клеток линии МА-104 после контакта с субстанцией препарата Арекур на протяжении 24 ч; контроль ВПГ-1/2 – количество клеток линии МА-104 через 24 ч после инфицирования вирусом ВПГ-1/2; антивирусная активность ФР – количество клеток линии МА-104 после инфицирования вирусом ВПГ-1/2 и обработки клеток ФР на протяжении 24 ч; анти ВПГ-1/2 активность субстанции препарата Арекур – количество клеток линии МА-104 после инфицирования вирусом ВВС и обработки клеток субстанцией препарата Арекур на протяжении 24 ч; % живых клеток – количество адгезированных живых клеток линии МА-104 относительно интактных, принятых за 100%.
Применения субстанции препарата Арекур в модельной системе МА-104/ВПГ-1/2 демонстрирует четкое концентрационно-зависимое влияние на жизнеспособность клеток: концентрация 500 мкг/мл обеспечивает 100% сохранность монослоя, тогда как двукратное уменьшение количества исследуемого вещества (до 250 мкг/мл) сопровождается уменьшением количества живых адгезированных клеток в исследуемых лунках более чем на 2/3. То есть, ЕС50 субстанции препарата Арекур составляет 300 мкг/мл. Как и в случае исследований на модельной системе L929/ВВС, токсическая концентрация СС50 субстанции препарата Арекур не определена. Поэтому расчет ХТИ можно провести только ориентировочно: >500/300 = >1,7. Полученная величина является непоказательной, хотя и неокончательной. Для аргументации того, что субстанция препарата Арекур имеет значимую анти ВПГ-1/2 активность, необходимо дополнительно провести определение СС50 препарата, используя стоковые концентрации. Полученные результаты обобщены в Табл. 1.
Таблица 1. Показатели токсичности и антивирусной активности субстанции препарата Арекур in vitro против РНК-содержащего вируса (ВВС) и ДНК-содержащего вируса (ВПГ-1/2)
| Модельная система | СС50 | ЕС50 | ХТИ (ІС) |
| L929/ВВС | > 500 | 10 | >50 |
| МА-104/ВПГ- 1/2 | >500 | 300 | >1,7 |
Таким образом, изучение антивирусной активности субстанции препарата Арекур in vitro против РНК-содержащего вируса (ВВС) и ДНК-содержащего вируса (ВПГ-1/2) с применением в качестве растворителя физиологического раствора позволило подтвердить предварительные результаты по активности препарата Арекур.
Выводы:
- Субстанция препарата Арекур проявляет выраженное антивирусное действие в модели L929/ВВС (РНК-вирус) и умеренное в модели МА-104/ВПГ-1/2 (ДНК-вирус).
- Указанный эффект в модельной системе Л929/ВВС (РНК-вирус) показателен: ХТИ субстанции препарата Арекур составляет >50 (указанная величина может быть скорректирована в сторону увеличения путем тестирования более высоких (чем использовано в исследовании) концентраций субстанции препарата.
- В модельной системе МА-104/ВПГ-1/2 (ДНК-вирус) ЕС50 в 30 раз больше, чем в модельной системе Л929/ВВС (РНК-вирус), что свидетельствует в пользу умеренной противовирусной антигерпетической эффективности исследованной субстанции препарата Арекур. Это закономерно, так как ДНК-геномные вирусы, такие как вирус герпеса, в процессе эволюции значительно позже РНК-геномных. Соответственно, более выраженная противовирусная активность МНP (mountain honey peptides), в том числе дефензина, апидаэцина и RJP-1 была изначально сформирована по отношению к более эволюционно древним РНК-вирусам. Это важно для клинической перспективы лечения социально значимых заболеваний: cезонных риновирусных инфекций (ОРВИ), клещевого энцефалита, болезни Коксаки, лихорадки Эбола, коронавирусной инфекции, гепатита С и др.
- Поскольку ХТИ в модельной системе МА-104/ВПГ-1/2 (ДНК-вирус) составляет >1,7, указанное значение можно уточнить в сторону увеличения после тестирования более высоких (чем взято в исследование) концентраций субстанции препарата.
- В обеих модельных системах, L929/ВВС (РНК-вирус) и МА-104/ВПГ-1/2 (ДНК-вирус), для образца субстанции препарата Арекур СС50 определить не удалось, поскольку концентрация 500 мкг/мл не вызывала каких-либо изменений в монослое клеток за 24 часа. Таким образом, можно сделать вывод об отсутствии токсичности субстанции препарата Арекур в представленных концентрациях.